Gen-Therapie erzeugt neue Nervenzellen zur Behandlung der Huntington-Krankheit
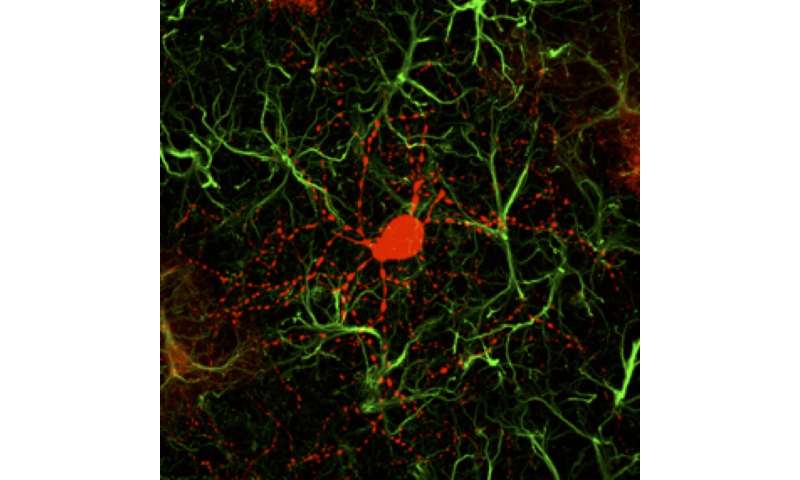
Die Huntington-Krankheit (HD) ist eine seltene Erkrankung, die durch abnorme chorea Bewegung und verursacht durch das Huntingtin (Htt) – gen-mutation und neurodegeneration in einer Hirnregion namens striatum. Eine Forschergruppe um Dr. Gong Chen, ein ehemaliger professor an der Penn State University und führt eine Gehirn-Reparatur-center an der Jinan Universität in China hat eine neuartige gen-Therapie zur Regeneration der funktionellen neuen Neuronen in Maus-Modellen HD. Die Arbeit wurde veröffentlicht in Nature Communications, Februar 27, 2020.
Wir sind mit der Entwicklung einer Reihe von NeuroD1-basierte gen-Therapien neu zu Programmieren Gehirn-interne Gliazellen, die direkt in funktionellen neuen Neuronen für die Behandlung einer Reihe von Gehirnstörungen, einschließlich der Huntington-Krankheit, Alzheimer-Krankheit, Schlaganfall, ALS, und viele mehr,“ sagte Dr. Chen. „Weil jedes einzelne neuron in unserem Gehirn ist umgeben durch die Unterstützung von Gliazellen, solche direkten glia-zu-neuron-conversion-Technologie bietet große Vorteile gegenüber der Stammzelltransplantation Therapie in Bezug auf die hohe Effizienz der neuroregeneration und keine sorgen über immunorejection,“ Dr. Chen Hinzugefügt.
Dr. Chen ist einer der frühen Pioniere Nutzung des internen brain Glia-Zellen, sich zu regenerieren funktionellen neuen Neuronen durch overexpressing neural Transkriptionsfaktoren im Gehirn der Maus. NeuroD1 (neurogene Differenzierung 1) ist ein solcher Faktor, der fördert die neuronale generation während der normalen Entwicklung des Gehirns. Chens team hat vorher gezeigt, dass die expression von NeuroD1 im Gehirn der Maus kann direkt konvertieren kortikalen Astrozyten (einer Unterform der Gliazellen) in funktionelle Neuronen (Guo et al. Cell Stem Cell, 2014; Chen et al. Molekulare Therapie, 2019; Zhang et al., BioRxiv, 2018). Vor kurzem, Chen ‚ s Gruppe weiter gemeldet, für das erste mal, dass eine solche direkte Astrozyten-zu-neuron-Konvertierung erfolgreich reproduziert in nicht-menschlichen Primaten-Gehirn (Ge et al., BioRxiv, 2019).
Chens team hat zuvor festgestellt, dass NeuroD1-generierten Neuronen sind hauptsächlich glutamatergen Neuronen, die für mehr als 80% der gesamten Neuronen im menschlichen Gehirn und sind die treibende Kraft der Aktivität des Gehirns. Aber HD ist, verursacht durch die degeneration von GABA-Ergen Neuronen, die eine Art von hemmenden Neuronen, die für mehr als 90% der Neuronen im striatum region. „Zur Erzeugung von Gabaergen Neuronen verbunden, NeuroD1, zusammen mit einem anderen transkriptionsfaktors Dlx2, von dem bekannt ist, generieren GABA-Ergen Neuronen während der frühen Entwicklung des Gehirns und erfolgreich umgewandelt striataler Astrozyten in GABA-Ergen Neuronen in HD-Mäuse,“ sagte der erste Autor dieses Artikels Dr. Zheng Wu. „Wichtig ist, hier haben wir das adeno-assoziierte virus (AAV) – Vektoren, die von der FDA zugelassen als eine gemeinsame Gentherapie-Vektor, der in vielen klinischen Studien zur Entwicklung eines neuartigen Gentherapie zur Behandlung der HD,“ Dr. Wu betonte, in der AAV-Gentherapie-Ansatz.
In diesem HD-Maus Studie, Dr. Chen und Kollegen berichteten, dass 80% der AAV-infizierten striatal Astrozyten wurden direkt umgewandelt in GABA-Ergen Neuronen und die restlichen Astrozyten können sich vermehren zu regenerieren sich. Im wesentlichen alle der neu generierten Neuronen sind electrophysiologically funktional, bilden synaptische verbindungen mit anderen Neuronen. Sie zeigt, dass die neu generierten Neuronen, die Ihre Axone projizieren können, um das richtige Ziel zu Gebieten, was darauf hindeutet, dass Sie haben, integriert in die Globale schaltkreise im Gehirn. „Die spannendsten Ergebnisse dieser HD-Untersuchung sind der wesentliche motor der funktionellen Erholung und Bemerkenswerte Verlängerung der Lebensdauer bei der gen-Therapie behandelten HD-Mäuse,“ sagte Chen.



