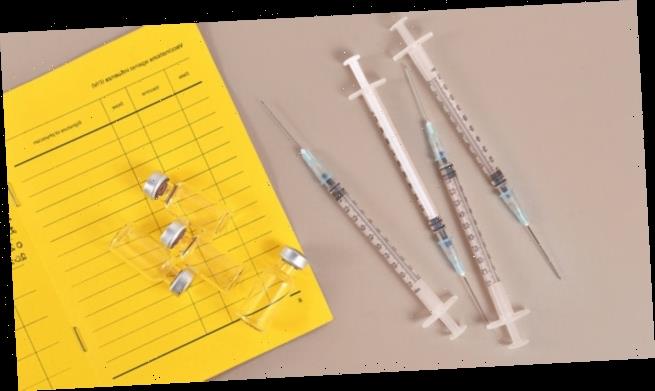
Eine Anleitung zur Handhabung der neuen und alten COVID-19-Impfstoffe
Das Gesundheitswesen startet in die neue „Impfsaison“ – mit neuen Impfstoffen. Die aktuelle DAZ hat für Sie zusammengefasst, was Apotheker:innen zur Handhabung und Lagerung wissen müssen. Denn schon die Bezeichnung auf den neuen Vials könnte so manchen verwirren.
Vergangenen Mittwoch hat der Deutsche Apothekerverband (DAV) die Apothekerkammern in einem Rundschreiben über abweichende Produktbezeichnungen bei den neuen COVID-19-Impfstoffen informiert. Die Firmen Biontech und Moderna hätten kurzfristig mitgeteilt, dass sowohl die Faltschachteln als auch die Durchstechflaschen der variantenangepassten COVID-19-Impfstoffe Produktbezeichnungen tragen, die nicht mit den Bezeichnungen aus der Fachinformation übereinstimmen.
Damit gemeint sind die Impfstoffe „Comirnaty Original / Omicron BA.1“ und „Spikevax Bivalent Original/Omicron BA.1“ – unter diesen Namen hat sie die europäische Arzneimittelbehörde EMA zur Zulassung empfohlen. Während sich diese Bezeichnung so auch in der Fachinformation wiederfindet – nämlich mit „Comirnaty® 15/15 µg/Dosis (Original/Omicron BA.1)“ und „Spikevax® 0,10 mg/ml (Original/Omicron BA.1)“ sollen auf den Etiketten der Vials Namen stehen, die so manchen verwirren könnten: „COMIRNATY tozinameran/riltozinameran 15/15 mcg“ und „Spikevax 0,10 mg/mL 0 / O“. Die Beschriftung der Vials sei zudem durchgängig auf Englisch. Der Grund: Mit der Herstellung der Impfstoffe wurde bereits vor Erteilung der Zulassung durch die EMA begonnen.
Mehr zum Thema

Breite Palette an Corona-Impfstoffen stellt neue Anforderungen an Handhabung und Lagerung
Start in die neue COVID-19-Impfsaison
EMA und ECDC
Vorerst nur Risikogruppen mit an Omikron BA.1 angepassten Corona-Impfstoffen impfen
Was es sonst noch zu beachten gilt, hat Apotheker Christian Heckmann in der aktuellen DAZ für Sie zusammengestellt. Er hat das Impfzentrum des Landkreises Kassel mit aufgebaut und betreut es nach wie vor pharmazeutisch. Zu den neuen angepassten bivalenten Impfstoffen erklärt er: „Beide Präparate setzen wie gehabt auf mRNA-Technologie, wobei nun zwei verschiedene mRNA-Sequenzen in jedem der Impfstoffe enthalten sind, 50 Prozent der Ursprungs-mRNA (15 µg Tozinameran [Biontech] bzw. 25 µg Elasomeran [Moderna]) und 50 Prozent der an die Omikron-BA.1-Variante angepassten mRNA (15 µg Riltozinameran [Biontech]; 25 µg Imelasomeran [Moderna]). Bei der Stabilität und beim grundsätzlichen Handling bleiben sich die Hersteller treu und orientieren sich an den uns bereits bekannten und zugelassenen Wuhan-Impfstoffen.“
Sorgfalt und Wachsamkeit
Jedoch müsse hinsichtlich der Logistik bei Biontech mit besonderer Sorgfalt und Wachsamkeit gearbeitet werden: „Leider gleichen die ‚neuen‘ Vials, abgesehen von der Bezeichnung auf dem Etikett, sehr stark der Fertiglösung des herkömmlichen Wuhan-Comirnaty-Impfstoffes (graue Kappe und graues Design). Diese Information muss auch besonders in den Arztpraxen bei Anlieferung verbreitet werden, damit Anwendungs- und Handhabungsfehler und damit potenzielle Falschimpfungen vermieden werden“, betont Heckmann.
Vielfalt als Schlüsselelement der Impfstrategie
EMA empfiehlt an Omikron BA.1 angepasste Corona-Impfstoffe zur Zulassung

Zulassung Ende der Woche erwartet
Angepasste COVID-19-Impfstoffe wohl ab der kommenden Woche bestellbar
Auch Moderna überrasche hinsichtlich der Haltbarkeit und Stabilität nicht. Jedoch finde sich seit einiger Zeit auch in der Fachinformation des Wuhan-Spikevax eine interessante Passage, worüber das Paul-Ehrlich-Institut momentan noch grübele, ob diese auch für die bereits produzierten und in Verkehr gebrachten Chargen angewendet werden kann. Diese Passage habe auch Einzug in die Fachinformation des nun bei uns eintreffenden bivalenten Spikevax erhalten: „Neuere Stabilitätsdaten des Herstellers erlauben die Vergabe einer maximalen Haltbarkeit von zwölf Monaten nach Herstellung (-50 °C bis -15 °C), sofern der Impfstoff nach dem Auftauen innerhalb von maximal 14 Tagen verwendet wird.“
Hier sei es nun sehr wichtig, genau auf aufgebrachte Hinweise und die Informationen auf dem Anlieferbeleg des Großhandels zu achten und diese wichtigen Informationen auch an die zu beliefernden Stellen weiterzugeben. „Zum einen ist es erfreulich, dass (mit Veröffentlichung dieser weiterführenden Stabilitätsdaten) der Impfstoff länger verwendet werden kann und damit nicht entsorgt werden muss, zum anderen darf die nun auf 14 Tage reduzierte Haltbarkeitsdauer bei ‚Kühlschranktemperatur‘ aus Gründen der Arzneimittelsicherheit und etwaigen Haftungsfragen nicht überschritten werden (§ 8 Abs. 3 Arzneimittelgesetz)“, erklärt Heckmann.

STIKO zu vierter Impfung, Nuvaxovid und PrEP mit Evusheld
Menschen ab 60 sollen nicht auf angepassten COVID-19-Impfstoff warten

Wissenswertes für Corona-Impfungen in der Apotheke
Es geht los!
Alle nach momentanem Stand verfügbaren Impfstoffe finden Sie in der DAZ 36/2022 in einer Tabelle zusammengefasst. Dabei wurde jedoch bewusst auf die 0,1 mg/ml Vials und Fertigspritzen von Wuhan-Spikevax und auf Vaxzevria verzichtet, um die Übersicht zu behalten. Es ist noch unklar, ob und wann die weiteren Formulierungen des Wuhan-Spikevax zu uns in die Apotheken kommen, Vaxzevria ist seit Ende des vergangenen Jahres in Deutschland nicht mehr verfügbar.
Quelle: Den ganzen Artikel lesen