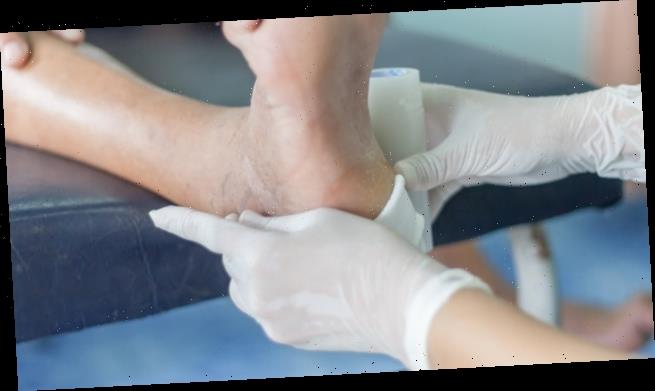
Betablocker-Gel bessert diabetische Fußulzera
Fußulzera bei Diabetikern heilen schwer ab und können derzeit nur konservativ versorgt werden. Der indische Hersteller Novalead Pharma präsentierte nun auf einem Kongress Ergebnisse für eine mögliche Pharmakotherapie mit einem Esmolol-haltigen Gel (Galnobax). Mit dem Topikum heilten die Fußulzera von Betroffenen deutlich besser ab. Der Effekt schien nachhaltig und das Gel nebenwirkungsarm.
Patienten, die unter dem diabetischen Fußsyndrom leiden, stehen derzeit nur wenige Therapieoptionen zur Verfügung. Eine konservative Wundbehandlung der Fußulzera gegebenenfalls in Verbindung mit einer Reinigung des Wundbetts (Debridement) bilden die Grundpfeiler der Therapie. Betroffene Areale werden außerdem durch spezielle Orthesen und Einlagen entlastet, um die Heilung zu fördern.
Mehr zum Thema

Alternative zu systemischer Propranolol-Therapie im Test
Topisches Timolol gegen Hämangiome?

Glaukomwirkstoff Timolol
Mit Augentropfen Migräne lindern

Diabetischer Fuß: Wachstumsfaktor fördert die Wundheilung

Ein neues Anwendungsgebiet für einen „alten“ Betablocker?
Weniger Melanom-Rezidive unter Propranolol
Pharmakologische Behandlungsoptionen, abgesehen von einer Antibiose bei möglichen Infektionen des ulzerierten Gewebes, existieren hingegen nicht. Der indische Hersteller Novalead Pharma möchte mit einem Esmolol-haltigen Gel diese Lücke füllen. Auf der Jahrestagung der European Association for the Study of Diabetes (EASD) 2022 in Stockholm präsentierte Ashu Rastogi für den Hersteller Phase-III-Daten zu dem Esmolol-haltigen Gel Galnobax®, das den Wunderverschluss beim diabetischen Fußsyndrom deutlich verbessern soll [1].
Drug Repurposing
Auf den ersten Blick mag man überrascht sein, ist Esmolol hierzulande schließlich als Infusionslösung (z. B. Brevibloc®) bei Tachykardie und Hypertonie zugelassen. Die Idee für die Umnutzung des Wirkstoffes (Drug Repurposing) entwickelten Kulkarni und Kollegen in silico, also im Computermodell, das vorhersagte, dass Esmolol das Enzym Aldose-Reduktase inhibieren kann [2].
Für die Pathogenese des diabetischen Fußsyndroms nimmt dieses Enzym des Polyol-Stoffwechselwegs eine Schlüsselrolle ein. Bei zu viel Glucose im Blut konvertiert die Aldose-Reduktase das Zuckermolekül zu Sorbitol, welches in weiteren Schritten zu Fructose und seinen reaktiven Metaboliten umgewandelt wird. Mit körpereigenen Proteinen reagieren die Zucker zu sogenannten fortgeschrittenen Glykierungsendprodukten (advanced glycation end products), die mit der gestörten Wundheilung bei Diabetes-Patienten in Verbindung gebracht werden [3]. In Laborversuchen inhibierte Esmolol die relevante Aldose-Reduktase und reduzierte die Glykierungsprodukte [2]. Den Wundverschluss bei diabetischen Ratten beschleunigte das Gel zwar nicht, beeinflusste aber verschiedene Surrogatparameter der Wundheilung [2].
Aussichtsreiche Phase-III-Ergebnisse
In der indischen Phase-III-Studie mit 251 Probanden mit länger als vier Wochen bestehenden Fußulzera fielen die Ergebnisse für das Galnobax®-Gel (14% Esmolol-Hydrochlorid) dafür deutlich aus [1]. Nach einer zwölfwöchigen Behandlung mit dem topischen Betablocker zusätzlich zur herkömmlichen Standardbehandlung verheilten die Fußulzera bei 41 von 68 Probanden (60,3%), während von den 72 Teilnehmern in der Kontrollgruppe mit der herkömmlichen Standardbehandlung nur 30 (41,7%) einen vollständigen Wundverschluss zeigten. Die Chance, dass die Wunde verheilte, war mit dem Gel mehr als doppelt so groß (Odds Ratio = 2,13; 95%-Konfidenzintervall = 1,08 bis 4,17; p = 0,0276). Zudem schienen die Ergebnisse von Dauer zu sein. Bei einem Follow-up-Termin in Woche 24 präsentierten 77,2% der Teilnehmer in der Esmolol-Gruppe und nur 55,6% der Probanden in der Kontrollgruppe einen erfolgreichen Wundverschluss.
Esmolol-Gel in der Rezeptur?
Ob der Hersteller eine Zulassung des Esmolol-Gels in Europa anstrebt, ist noch unklar. Esmolol-haltige Gele könnten Apotheken aber als Rezepturarzneimittel herstellen. Das Galnobax®-Gel nutzt das Poloxamer Pluronic F 108 NF Prill als Gelbildner sowie Benzalkoniumchlorid zur Konservierung [5]. Auch andere Hydrogelformulierungen beispielsweise mit nichtionischen Celluloseethern als Gelbildner sollten prinzipiell geeignet sein, denn in wässriger Lösung zeigte sich der Wirkstoff stabil [6].
Die Vorteile des Gels bestanden unabhängig von Art sowie Ausdehnung der Ulzera und unabhängig von Risikofaktoren wie einem hohen Body Mass Index bzw. HbA1c-Wert. Einziger Wermutstropfen: Die Studie enthielt eine zweite, kleinere Kontrollgruppe, die neben der Standardbehandlung ein Placebo-Gel erhielt. Die Ergebnisse dieser Teilnehmer sind leider im Kongress-Abstract nicht publiziert. Zu den Nebenwirkungen zählen laut der vorangegangenen Phase-I/II-Studie lokale Hautreaktionen [4]. Die systemische Esmolol-Exposition durch das Gel lag zu jedem Zeitpunkt der Untersuchung unter der Nachweisgrenze [4].
Literatur
[1] Rastogi A et al. Novel topical esmolol hydrochloride for diabetic foot ulcer: phase 3, randomised, double-blind, placebo-controlled, multi-centre study. Vortrag auf der 58. Jahrestagung der European Association for the Study of Diabetes, 20. September 2022, Stockholm, www.abstractsonline.com/pp8/#!/10613/presentation/354
[2] Kulkarni SA et al. Novel topical esmolol hydrochloride improves wound healing in diabetes by inhibiting aldose reductase, generation of advanced glycation end products, and facilitating the migration of fibroblasts. Front Endocrinol 2022;13:926129, doi: 10.3389/fendo.2022.926129
[3] Takeuchi M. Toxic AGEs (TAGE) theory: a new concept for preventing the development of diseases related to lifestyle. Diabetol Metab Syndr 2020;12(1):105, doi: 10.1186/s13098-020-00614-3
[4] Rastogi A et al. Novel topical esmolol hydrochloride (Galnobax) for diabetic foot wound: phase 1 /2, multicentre, randomized, double-blind, vehicle-controlled, parallel-group study. Adv Wound Care 2022. doi: 10.1089/wound.2022.0093
[5] Kulkarni SA et al. Topical Formulation for Diabetic Foot Ulcers. Patent der World Intellectual Property Organization, Internationale Antragsnummer: PCT/IN2010/000637, 7. April 2011, www.surechembl.org/document/WO-2011039780-A2
[6] Baaske DM et al. Stability of esmolol hydrochloride in intravenous solution. Am J Hosp Pharm 1994;51:2693-2696
Quelle: Den ganzen Artikel lesen